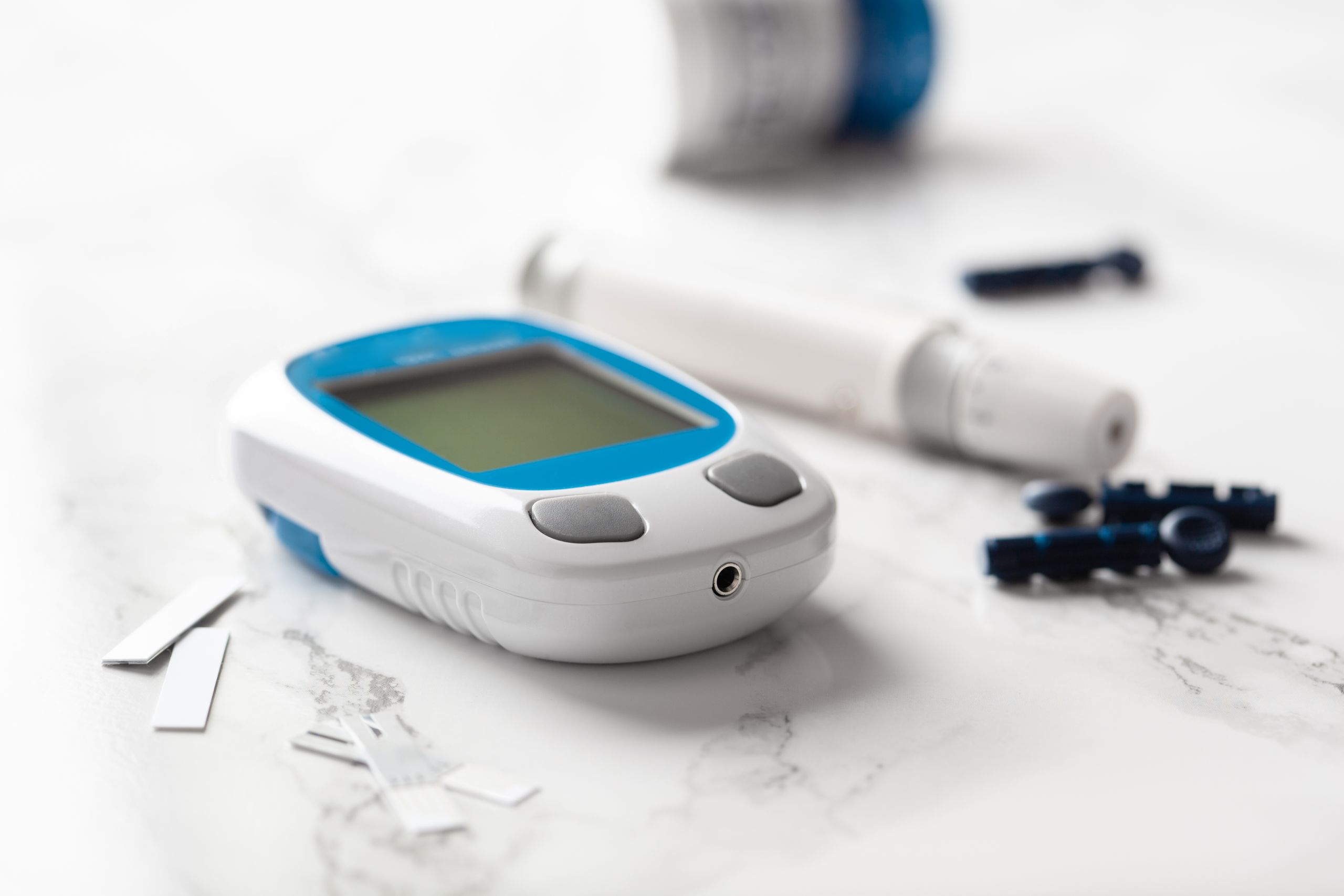
A regulamentação da Anvisa entrou em vigor no início de março. E a expectativa é que os pacientes possam comprar os produtos com mais facilidade a partir do próximo mês
A espera foi longa, mas a Cannabis medicinal está muito perto de ajudar um número cada vez maior de pessoas no Brasil. Em dezembro de 2019, a Agência Nacional de Vigilância Sanitária (Anvisa) definiu que empresas farmacêuticas poderão importar ou produzir produtos à base de Cannabis, e comercializá-los em farmácias.
Os primeiros produtos devem chegar às prateleiras das farmácias entre maio em junho. A resolução da Anvisa, publicada em dezembro, levou 90 dias para entrar em vigor. E, desde março, as empresas interessadas no negócio já podem pedir o registro dos produtos. O primeiro deles foi aprovado no dia 22 de abril. Trata-se de um fitofármaco que possui canabidiol e concentração inferior a 0,2% de THC, da empresa paranaense Prati-Donaduzzi.
Disponível nos próximos meses
A expectativa do Conselho Federal de Farmácias (CFF) é a de que novos registros sejam publicados mês a mês. Entre o segundo semestre deste ano e o primeiro de 2021, espera-se que a oferta seja ampla. É importante lembrar que a resolução da Anvisa não fala em medicamentos, mas em produtos. É assim que a Cannabis medicinal estará no mercado brasileiro por pelos menos três anos.
“A agência entendeu que não há estudos o suficiente comprovando a eficácia dessas fórmulas. Acreditamos também que há uma desconfiança em relação à matéria-prima, já que ela ainda não pode ser produzida e analisada aqui. Boa parte do que é importado hoje também vem como suplemento, e não medicamento. Isso é uma realidade em todo o mundo ainda”, explica Margarete Kish, professores, pesquisadora e coordenadora do grupo de trabalho sobre o uso medicinal de Cannabis sativa do CFF.
A distinção entre produto e medicamento traz implicações práticas. Farmácias de manipulação não poderão manipular as fórmulas, e só poderão vender os produtos se possuírem lojas conjugadas aos laboratórios. Já as exigências de estudos de estabilidade – tempo de validade em estoque e prateleiras, entre outros – são mais brandas para os produtos. Eles também não terão nome fantasia; o rótulo trará apenas o ingrediente base da fórmula, e nenhuma indicação de uso.
Mas como ter acesso?
A orientação aos médicos é que a Cannabis medicinal seja usada quando outros tratamentos não tenham bons resultados. A tendência, segundo Kish, é que com mais produtos disponíveis a formação médica sobre o tema também aumente. Os produtos só serão vendidos sob prescrição, com a receita do tipo B, com numeração controlada pela Anvisa, com validade de até 60 dias e retenção de uma via.
Dosagem, frequência do uso e fórmula mais adequada também deverão ser indicadas pelos médicos. Além da farmácias, os produtos também estarão disponíveis em hospitais, clínicas e postos de saúde, de acordo com a demanda. Devido à pandemia de Covid-19 os médicos poderão enviar o receituário online, ou combinar com os pacientes a melhor forma de enviar as receitas.
O CFF afirma que o abastecimento das farmácias será de responsabilidade de cada fornecedor, como já ocorre. As farmácias, por sua vez, terão que cumprir as exigências da Anvisa, que é a mesma para outros produtos já comercializados. Portanto, não terão que se adequar a nenhuma nova regra.
A resolução que regulariza a produção e comercialização da Cannabis medicinal no país ainda é incipiente. Não trata de questões importantes, como o cultivo da planta. Mas é um importante avanço para quem precisa do tratamento.