A expectativa para 2023 é que avanços robustos aconteçam no setor da Cannabis no Brasil, como a atualização da RDC 327/2019 por exemplo. Mas antes de colocar os pés neste novo ano, é necessário fazer um balanço sobre os últimos doze meses. Para isso, conversamos com o gerente de Medicamentos Específicos, Notificados, Fitoterápicos, Dinamizados e Gases Medicinais (GMESP) da Anvisa, João Paulo Silverio Perfeito.
Balanço de 2022: 25 produtos de Cannabis aprovados pela Anvisa por meio da RDC 327/2019 e com mais de 65.595 autorizações de importação de produtos de Cannabis por via da RDC 660
“Terminamos o ano com 25 produtos de Cannabis aprovados pela Anvisa por meio da RDC 327/2019: 14 contendo canabidiol e 11 à base de extratos de Cannabis sativa.
Foi um ano de muita discussão, avanços e amadurecimento em relação ao assunto. Além de várias reuniões técnicas que aconteceram durante 2022, a Anvisa participou de vários eventos, nacionais e internacionais, onde foi possível apresentar o nosso marco regulatório sobre o tema, discutir e conhecer melhor outros modelos regulatórios de autoridades de referência internacional em saúde”.

João Paulo Perfeito conversou com o Cannabis & Saúde sobre 2022 e expectativa para 2023.
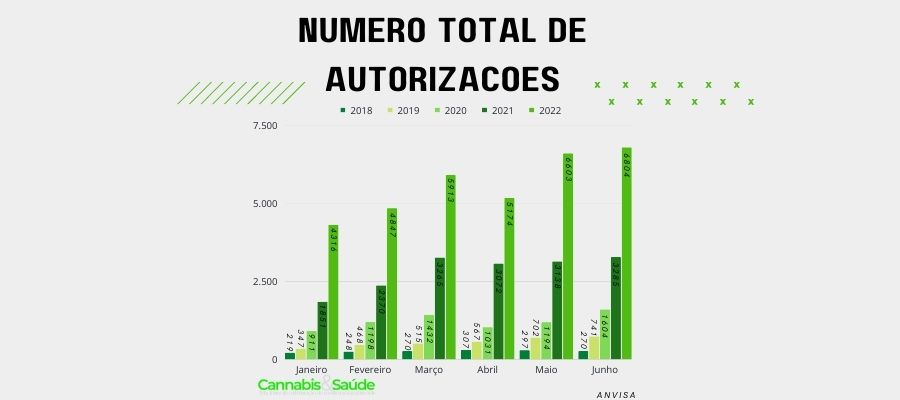
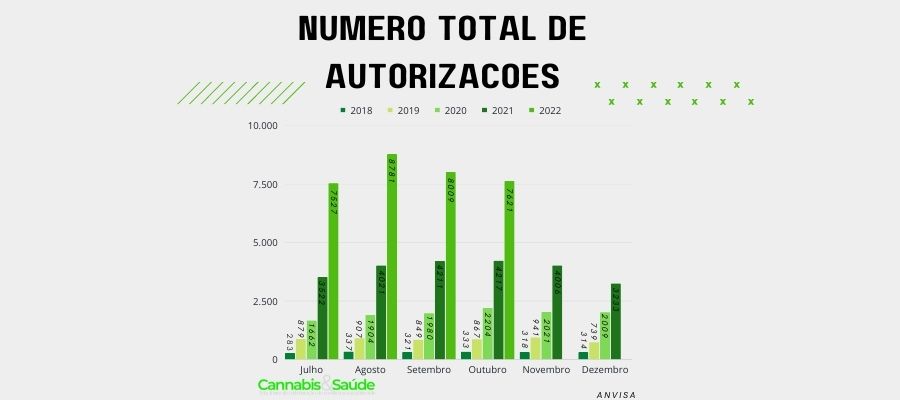
Importações: até outubro foram 65.595 autorizações de importação de produtos de Cannabis via da RDC 660
Os números de importações cresceram a cada ano no Brasil. Conforme dados da Anvisa, até outubro de 2022 aconteceram 65.595 autorizações de importação de produtos de Cannabis via a RDC 660. Neste mesmo período em 2021 o número foi de 32.997.

Sobre a a RDC n° 660/2022, Perfeito afirma que:
“Esta resolução define os critérios e os procedimentos para a importação, em caráter excepcional, de Produto derivado de Cannabis, por pessoa física, para uso próprio, mediante prescrição de profissional legalmente habilitado, para tratamento de saúde.
Trata-se de produtos para os quais não foram avaliados dados de segurança e eficácia. Portanto, não são considerados medicamentos, não sendo adequado que os mesmos sejam referenciados dessa forma”.
Revisão da RDC 327 deve acontecer logo no início de 2023
Em relação à revisão da RDC 327, Perfeito explicou que foi decidido priorizar a participação social dos interessados no assunto. E por isso, com um viés democrático, abriu-se a consulta pública para que toda a sociedade pudesse participar de alguma maneira neste processo regulatório:
“O tema foi inserido na Agenda Regulatória 2021-2023 da Anvisa, contemplado no Projeto nº 8.37, e foi aberto o Processo regulatório SEI nº 25351.912833/2022-80 a partir do Termo de Abertura (TAP) nº 46 de 23/05/2022 e iniciada as discussões de Análise do Impacto Regulatório (AIR) entre as áreas da Anvisa relacionadas ao tema.
O processo de regulação prevê a realização de AIR, a qual contempla mecanismos de participação social e a elaboração do Relatório correspondente.
A realização da AIR faz-se obrigatória em atendimento ao art. 6º da Lei nº 13.848/2019 (Lei das Agências) e art. 5º da Lei nº 13.874/2019 (Lei da Liberdade Econômica). Neste sentido, foi decidido pela importância de se privilegiar a participação social dos interessados desde o início deste processo regulatório, tendo sido realizado nos meses de outubro e novembro o e-participa, aberto a todos os interessados, com o objetivo de coletar informações, dados e evidências sobre os assuntos em discussão.
As contribuições recebidas serão consolidadas e farão parte do Relatório de AIR. As etapas subsequentes incluem a elaboração da proposta de texto normativo, divulgado na forma de Consulta Pública (CP), consolidação e análise das contribuições recebidas, elaboração do instrumento final, análise jurídica, deliberação pela Diretoria Colegiada da Anvisa (Dicol) e publicação da nova Resolução aprovada no DOU. Desta forma, seguindo o rito regulatório em andamento, esperamos em breve avançar com a conclusão da revisão da RDC 327/2019”.
Entenda a diferenças entre a RDC 327 e a RDC 660
“As duas normas visam possibilitar o acesso de pacientes sem outras alternativas terapêuticas, e que podem se beneficiar desse uso, aos produtos medicinais à base de Cannabis.
A resolução RDC 327 trata da regularização dos produtos para o mercado brasileiro. A resolução RDC 660 trata da importação excepcional para uso pessoal.
Os produtos aprovados por meio da RDC 327/2019 podem ser fabricados no Brasil ou importados, e passam por avaliação prévia da Anvisa em relação ao seu processo produtivo e qualidade. Eles podem ser comercializados no Brasil por farmácias e drogarias a partir de prescrição médica.
Já os produtos cuja importação é autorizada por meio da RDC 660/2022, não passam por avaliação prévia da Anvisa concernente a estes aspectos. Estes produtos podem ser importados a partir de prescrição médica e solicitação de importação individual junto à Anvisa”.
Ações mais relevantes no setor da Cannabis no Brasil
Por fim, em termos de ações, no âmbito regulatório brasileiro, Perfeito destacou cinco importantes acontecimentos:
- A aprovação de mais 16 produtos de Cannabis pela Anvisa em 2022, chegando ao total de 25 produtos aprovados;
- A aprovação pela Diretoria Colegiada da Anvisa do entendimento da área técnica, que possibilita, em caráter excepcional, a importação de derivado vegetal de Cannabis spp. para purificação e obtenção, em território nacional, do fitofármaco canabidiol para ser usado na fabricação de produtos de Cannabis;
- O webinar sobre pesquisa clínica em Cannabis medicinal, realizado em maio pelas áreas técnicas da Anvisa (GMESP, COPEC e GPCON);
- A realização do e-participa, como etapa de participação social, visando a revisão da RDC 327/2019;
- A autorização da Anvisa concedida à UFRN para o cultivo de Cannabis para fins de pesquisa científica”.

















